炒股就看金麒麟分析師研報,權威,專業,及時,全面,助您挖掘潛力主題機會!
(來源:DeepTech深科技)
世界頂級合成生物大佬也開始研究 AI 課題,並利用 AI 生成了尚未被發現或壓根不存在的假設性化學分子。也就是說,AI 從零開始憑空創造出了任何數據庫中都不存在的全新分子結構,實現了抗生素的從頭設計。
 圖 | 詹姆斯·柯林斯(James Collins)教授(來源:資料圖)
圖 | 詹姆斯·柯林斯(James Collins)教授(來源:資料圖)具體來說,美國麻省理工學院詹姆斯·柯林斯(James Collins)教授和團隊將 AI 瞄準抗微生物耐藥性,為助力消滅超級細菌打造了一種「剋星」,即利用生成式 AI 設計出了可以殺滅耐藥菌的化合物。
研究中,他們利用生成式 AI 算法設計出超過 3600 萬個潛在化合物,並通過計算篩選它們的抗菌特性。藉此所發現的候選化合物在結構上與現有任何抗生素都是截然不同的,並且似乎能夠通過破壞細菌細胞膜的全新機制來發揮作用。這種方法使得他們能夠生成並評估前所未見的理論化合物,未來他們還希望能將這一策略用於識別和設計對其他細菌物種具有活性的化合物。
 (來源:Cell)
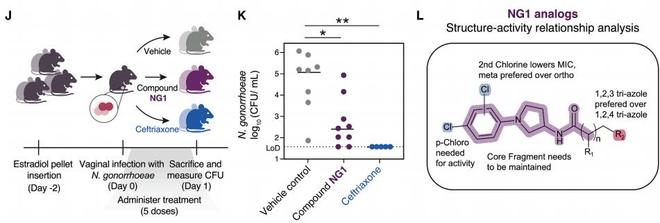
(來源:Cell)具體來說,他們開發了一個生成式 AI 框架,通過兩種策略實現了抗生素的從頭設計:其一是基於片段的虛擬篩選方法,針對淋病奈瑟菌和金黃色葡萄球菌系統性評估超過 1000 萬個化學片段,進而優化潛力片段;其二是無約束的化合物從頭生成策略,二者均採用遺傳算法與變分自編碼器技術。
在 24 種合成化合物中,7 種顯示出選擇性抗菌活性。其中兩種先導化合物對多重耐藥菌株具有殺菌效力,它們通過獨特的作用機制顯著降低了小鼠模型中淋病奈瑟菌陰道感染和耐甲氧西林金黃色葡萄球菌皮膚感染的細菌負荷。與此同時,本次研究還驗證了這兩類化合物的結構類似物同樣具備抗菌活性。
 (來源:Cell)
(來源:Cell)
微小殺手已在全球奪走數百萬人生命
儘管有人擔心 AI 終有一天會毀滅人類,但也許 AI 的崛起未必能置人類於死地,而耐藥性細菌卻會輕易地做到這一點。在全球範圍內,據估計耐藥性細菌感染每年導致近 500 萬人死亡。這些微小的殺手已經在全球奪走了數百萬人的生命,而有效的抗生素儲備卻在不斷減少。
在過去 45 年裏,美國食品藥品監督管理局(FDA,Food and Drug Administration)批准了幾十種新的抗生素,但其中大多數都是現有抗生素的變體。與此同時,細菌對於這類藥物的耐藥性卻在不斷增強。面對抗生素的耐藥性危機,人們亟需結構獨特的新型抗菌藥物。儘管深度學習技術能夠從現有化合物庫中篩選抗菌物質,但其結構新穎性始終受限。
為了找到新的抗生素來應對這一日益嚴峻的問題,柯林斯與麻省理工學院「抗生素-AI 項目」的其他研究人員藉助 AI 的力量,對龐大的現有化合物庫進行了篩選。在本次成果之前,這一系列工作已產出多個頗具潛力的候選藥物,包括哈立定(halicin)和阿鮑辛(abaucin)等。
為了在此基礎上更進一步,該團隊在本次研究中將目標鎖定在耐藥性淋病和多重耐藥性金黃色葡萄球菌上。耐藥性淋病被美國衛生官員稱為「緊迫的公共衛生威脅」;而對於多重耐藥性金黃色葡萄球菌包括耐甲氧西林金黃色葡萄球菌來說,人類通過接觸感染者或受污染的醫療設備就能感染這種細菌。
因此,該團隊希望通過探索化學空間中未被充分研究的領域來發現全新的作用機制,同時希望摒棄任何看似與現有抗生素相似的物質,從根本上以不同的方式助力解決抗菌耐藥性危機,所以他們將搜索範圍擴大到任何化合物庫中都找不到的分子。因此他們意識到,通過利用 AI 生成那些不存在或尚未被發現的假設性可能分子,有望探索到種類遠遠要豐富得多的潛在藥物化合物。
在本次研究中,他們採用了兩種不同的方法:其一,指導生成式 AI 算法基於具有抗菌活性的特定化學片段來設計分子;其二,讓算法自由地生成分子,無需包含特定片段。
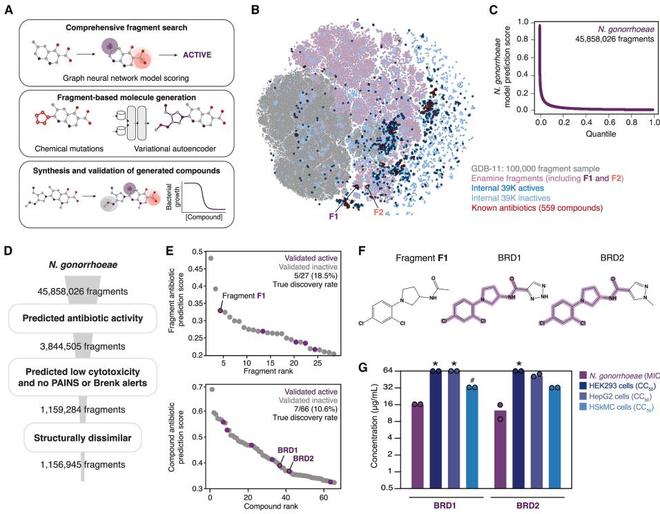
在基於片段的方法中,他們希望找到能夠殺滅淋病奈瑟菌的分子。為此,他們首先構建了一個包含大約 4500 萬個已知化學片段的庫,其中包括由碳、氮、氧、氟、氯、硫這 11 種原子的所有可能組合構成的片段,以及來自烏克蘭 Enamine 公司「易獲取(REAL,REadily AccessibLe)化學空間」的片段。
此前,柯林斯等人曾經訓練了一款機器學習模型,該模型可以預測針對淋病奈瑟菌的抗菌活性,於是他們使用這一模型針對上述化學片段庫進行篩選。通過篩選他們得到了將近 400 萬個片段。接着,他們進一步地縮小範圍,剔除了那些被預測結果認為對人體細胞具有細胞毒性、存在化學隱患以及已知與現有抗生素相似的片段,最終留下大約 100 萬個候選片段。
之所以這樣做,是因為需要摒棄任何看似與現有抗生素相似的物質,以便從根本上以不同的方式助力解決抗菌耐藥性危機。只有探索化學空間中未被充分研究的領域,才能發現全新的作用機制。
經過多輪實驗和計算分析之後,他們確定了一個名為 F1 的片段,這個片段似乎對於淋病奈瑟菌具有良好的抗菌活性。於是,他們以這個片段為基礎,利用兩種不同的生成式 AI 算法生成了更多化合物。
第一種算法名為「化學合理突變(CReM,chemically reasonable mutations)」,其工作原理是從包含 F1 的特定分子入手,通過添加、替換或刪除原子及化學基團來生成新分子。第二種算法是「基於片段的變分自編碼器(F-VAE,fragment-based variational autoencoder)」,它以化學片段為基礎構建完整分子,該算法通過對由歐洲生物信息學研究所維護的生物活性分子數據庫 ChEMBL 數據庫中的 100 多萬個分子進行預訓練,從而能夠學習片段常見的修飾模式,進而能夠完成分子構建。
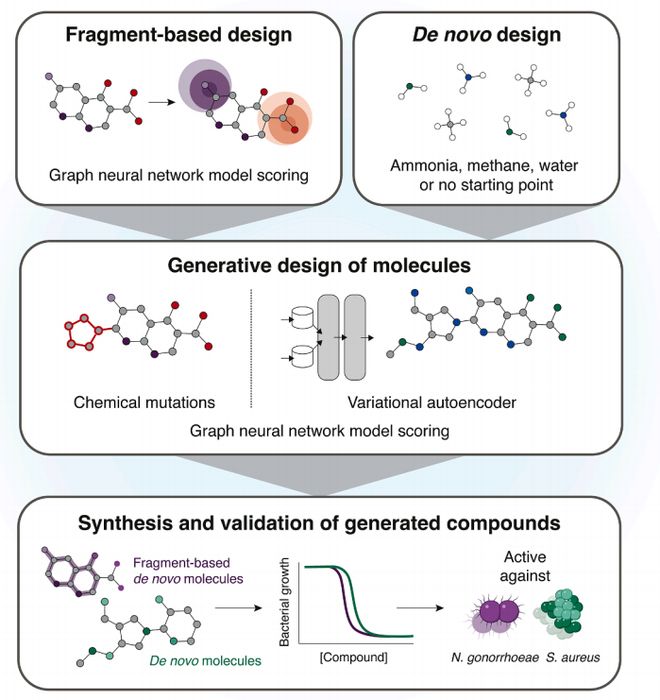
在這兩種算法的幫助之下,他們生成了大約 700 萬個包含 F1 的候選化合物,並通過計算來篩選它們對淋病奈瑟菌的活性。篩選之後他們得到大約 1000 種化合物,隨後從中選取 80 種提供給了化學合成供應商,並讓他們看看是否能夠合成,最終只有兩種能夠被合成。其中有一種名為 NG1 的化合物,無論是在實驗室培養皿還是在耐藥性淋病感染小鼠模型中,都能高效殺滅淋病奈瑟菌。
實驗表明,NG1 會與一種名為 LptA 的蛋白質相互作用,這種蛋白質是一種能夠參與細菌外膜合成的新型藥物靶點。據了解,這種藥物似乎能夠通過干擾膜合成來發揮作用,而膜合成受阻對於細菌細胞而言是致命的。

可能蘊藏着下一代拯救生命的藥物
與此同時,該團隊探索了利用生成式 AI 自由設計分子的潛力,這一次他們瞄準了革蘭氏陽性菌的代表菌種金黃色葡萄球菌。
期間,他們再次使用 CReM 和 VAE 來生成分子。但是,這一次他們除了遵循使用原子結合來形成化學上合理的分子的通用規則之外,沒有設定其他限制條件。結果,這些模型共同生成了超過 2900 萬個化合物。隨後,他們對針對金黃色葡萄球菌的候選化合物應用了與淋病奈瑟菌候選化合物相同的篩選標準,進而將候選庫縮減至約 90 種化合物。
通過此,他們成功合成並測試了其中 22 種分子,發現其中 6 種在實驗室培養皿中對多重耐藥性金黃色葡萄球菌展現出強大的抗菌活性。其還發現,其中有一種候選化合物 DN1 能夠在耐甲氧西林金黃色葡萄球菌皮膚感染的小鼠模型中清除感染。而且它似乎也能干擾細菌細胞膜,但是作用範圍更廣,而非侷限於與某一種特定蛋白質的相互作用。
 (來源:Cell)
(來源:Cell)另據悉,柯林斯同樣隸屬於「抗生素-AI 項目」的非營利組織 Phare Bio 的聯合創始人。目前,該組織正致力於對 NG1 和 DN1 進行進一步修飾,以便使其適用於更多測試。通過與 Phare Bio 的合作,該團隊正在探索類似的化合物,同時通過藥物化學工作推進最有潛力的候選化合物進入臨牀前階段。
總的來說,這一框架實現了生成式深度學習引導的抗生素從頭設計,為探索化學空間的未知領域提供了創新平台。也為抗生素研發開闢了新的可能性,從藥物設計的角度展現了 AI 的力量,讓人們得以探索以前無法觸及的更廣闊化學空間,而這片尚未被探索的領域可能蘊藏着下一代拯救生命的藥物。但是,抗生素的發現、開發和生產都必須是成本低廉的,因此未來如有機會規避與合成可行性相關的問題,將會為這一成果帶來更多優勢。
 (來源:Cell)
(來源:Cell)另據悉,柯林斯能夠成為合成生物學巨擘,也和自己的經歷息息相關。他出生於美國紐約市,10 歲時隨家人搬到新罕布什爾州。他的父親是一名航空工程師,曾參與美國國家航空航天局和軍方的項目。在兩位祖父輩的親人都身患殘疾——一位失明、另一位則多次中風之後,柯林斯對醫學工程產生了興趣。他曾告訴麻省理工學院官網:「我當時深受觸動——我們有那麼多了不起的技術能把東西發射到天上、從天上回收,卻幾乎沒有為這些老人做什麼來恢復他們失去的功能。」於是,在美國聖十字學院獲得物理學學士學位後,柯林斯前往英國牛津大學攻讀醫學工程。
1990 年,他加入美國波士頓大學任教,主要研究人類行走、跑步和平衡維持的機制。20 世紀 90 年代中期,同事們鼓勵柯林斯嘗試將自己的工程學和物理學專業知識應用到分子生物學領域,於是他與合成生物學的其他先驅者開始嘗試設計基因迴路並一直走到了今天。如今在麻省理工學院,他仍在改造病毒和細菌,並希望可以更好地造福人類。
參考資料:
https://www.emjreviews.com/microbiology-infectious-diseases/news/ai-designs-new-antibiotics-to-tackle-drug-resistant-bacteria/
https://news.ki.se/designing-novel-antibiotics-against-priority-pathogens-using-generative-ai
https://www.google.com.hk/search?hl=zh-CN&q=A+generative+deep+learning+approach+to+de+novo+antibiotic+design
https://www.sciencedirect.com/science/article/abs/pii/S0092867425008554
https://www.euronews.com/health/2025/08/15/mit-scientists-use-ai-to-develop-new-antibiotics-for-stubborn-gonorrhoea-and-mrsa
https://zh.wikipedia.org/wiki/%E8%A9%B9%E5%A7%86%E6%96%AF%C2%B7J%C2%B7%E6%9F%AF%E6%9E%97%E6%96%AF
https://news.mit.edu/2015/profile-james-collins-1114
https://stokedbio.com/team/
運營/排版:何晨龍